Tisagenlecleucel, das aus patientenindividuell hergestellten T-Lymphozyten mit einem chimären Antigenrezeptor (CAR-T-Zellen) gegen das CD19-Antigen auf lymphatischen Zellen besteht, wurde im August 2018 als Gentherapie zugelassen – für pädiatrische Patienten und junge Erwachsene mit akuter lymphatischer Leukämie von B-Zellen (B-ALL) und für Erwachsene mit diffus-großzelligem B-Zell-Lymphom (DLBCL). In beiden Indikationen müssen die Patienten mindestens zwei Rezidive nach systemischen Therapien – im Fall der ALL auch nach einer allogenen Stammzelltransplantation (alloSCT) – erlitten haben oder refraktär gegen Standardtherapien sein.
CAR-T-Zellen sind umprogrammierte, patienteneigene T-Lymphozyten, denen das Gen für einen chimären Antigenrezeptor (CAR) – bei Tisagenlecleucel gegen das CD19-Antigen – eingepflanzt wird. Das versetzt die Zellen in die Lage, CD19-tragende Tumorzellen zu erkennen, an sie zu binden und sie in der Folge zu eliminieren. Das Gen für den CAR enthält außerdem ko-stimulatorische Domänen, durch die Expansion und Persistenz der Zellen gesteigert werden.
Erfahrungen aus der Behandlung erwachsener Lymphom-Patienten
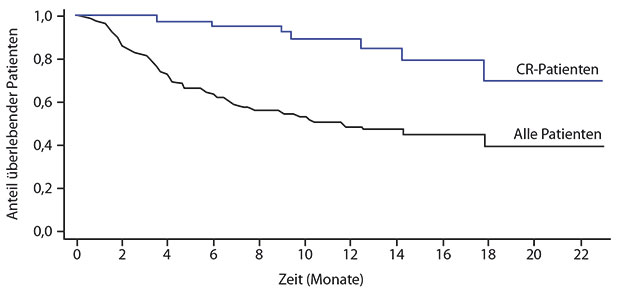
Laut Prof. Peter Borchmann, Köln, Leiter der klinischen Prüfung von Tisagenlecleucel bei DLBCL-Patienten in der JULIET-Studie, haben Patienten mit rezidiviertem oder refraktärem DLBCL mit konventionellen Therapien eine äußerst schlechte Prognose. Die Follow-up-Daten von JULIET zeigen, dass von den 111 Patienten 52% ansprachen, davon 40% mit einer kompletten und 12% mit einer partiellen Remission [1]. Nach zwölf Monaten betrug die Gesamtüberlebensrate 49% und die rezidivfreie Überlebensrate der Patienten in kompletter Remission 78,5%. Prognostisch wichtig scheint das Ansprechen nach drei Monaten zu sein: Patienten, die dann mindestens in partieller Remission waren, blieben zu 83% auch nach zwölf Monaten noch progressionsfrei. Eine initiale partielle Remission konnte im weiteren Verlauf in 54% der Fälle zu einer kompletten Remission konvertiert werden. Kein Patient unterzog sich in Remission einer alloSCT. Das mediane Gesamtüberleben aller Patienten lag bei 11,7 Monaten, bei den Patienten in kompletter Remission ist der Medianwert noch nicht erreicht (Abb. 1); mit konventionellen Therapien erreicht man etwa 4,4 Monate, so Borchmann.