Urogenitale Tumoren: Fortschritte in der Erst- und Zweitlinie beim Urothelkarzinom
In den USA wurde der PD-L1-Inhibitor Atezolizumab kürzlich für das Urothelkarzinom zugelassen, und in Kopenhagen gab es neue Daten zur Zweit- ebenso wie zur Erstlinienbehandlung mit
PD-1-Inhibitoren: So scheint Nivolumab, das für das fortgeschrittene, vorbehandelte Nierenzellkarzinom bereits zugelassen ist, auch beim metastasierten oder chirurgisch nicht resezierbaren, lokal fortgeschrittenen Urothelkarzinom effektiv zu sein. Nach vielversprechenden Phase-I/II-Daten erhielten in der einarmigen Phase-II-Studie CheckMate-275 insgesamt 270 Patienten mit platinresistentem Urothelkarzinom 3 mg/kg Nivolumab alle zwei Wochen bis zu Progression oder Therapieabbruch.
Die Ansprechrate war abhängig vom Ausmaß der PD-L1-Expression, so Matthew Galsky, New York [1]: Sie lag bei Tumoren mit ≥ 5% Expression bei 28,4%, bei Patienten mit geringerer Expression aber immerhin auch bei 15,8%. Die mediane Dauer des Ansprechens ist noch nicht erreicht, bei drei Viertel der Responder halten die Remissionen weiter an. Mit einer medianen progressionsfreien Zeit von zwei Monaten und einer medianen Gesamtüberlebensdauer von 8,74 Monaten sprechen die Autoren von einer klinisch relevanten Wirksamkeit der Therapie, die überdies mit etwa 18% Grad-3/4-Nebenwirkungen gut verträglich war. Die Zulassung für diese Indikation, für die therapeutische Optionen rar sind, wurde sowohl in den USA als auch in Europa beantragt.
Bereits in der Erstlinientherapie des fortgeschrittenen bzw. nicht resektablen Urothelkarzinoms ist der andere PD-1-
Antikörper, Pembrolizumab, angekommen: In der Phase-II-Studie KEYNOTE-
052 wurden 374 Patienten mit solchen Tumoren, die für eine Cisplatin-basierte Chemotherapie nicht infrage kamen, mit 200 mg Pembrolizumab alle drei Wochen für maximal zwei Jahre behandelt [2].
24% der Patienten erzielten eine Remission, die in 6% der Fälle komplett war. Bei hoher PD-L1-Expression lag auch die Ansprechrate höher; insbesondere erzielten hier doppelt so viele Patienten eine Komplettremission (13,3% vs. 6,3%). Nach median acht Monaten Follow-up, so Arjun Balar, New York, ist der Medianwert der Remissionsdauer noch nicht erreicht; für 83% der Responder liegt sie bei mindestens sechs Monaten. Bei nur 16% der Patienten wurden behandlungsbedingte Nebenwirkungen der Grade 3 oder 4 registriert, 5% brachen deshalb die Behandlung ab.
Verglichen mit historischen Kontrollen scheint das Ansprechen auf Pembrolizumab in der Erstlinie etwas geringer zu sein als auf eine Chemotherapie, aber die Dauer des Ansprechens auf Pembrolizumab könnte dafür länger sein. Mit Sicherheit, so Maria DeSantis, Warwick, haben die Immun-Checkpoint-Inhibitoren bereits angefangen, die therapeutische Landschaft bei diesen notorisch schwierig zu behandelnden Tumoren zu verändern. Für die kommenden Jahre seien hier dramatische Veränderungen zu erwarten.
Beim Nierenzellkarzinom erstmals Erfolg einer adjuvanten Therapie
Nur etwa ein Sechstel aller Nierenzellkarzinome ist bei Diagnose noch lokoregionär begrenzt, und auch das ist keine sehr gute Nachricht für diese Patienten: Etwa 40% von ihnen entwickeln nach kurativer Nephrektomie ein Rezidiv mit Fernmetastasen, und deshalb lebt nach fünf Jahren nur mehr etwa die Hälfte von ihnen. Je nach Rezidivrisiko lassen sich solche Patienten mithilfe des University of California at Los Angeles Integrated Staging System (UISS) und des Stage, Size, Grade, and Necrosis-Scores (SSIGN) in verschiedene Risikoklassen einteilen. Adjuvante Therapieversuche mit Zytokinen, Bestrahlung oder Hormontherapien waren bisher erfolglos. Obwohl anti-angiogene Therapien im metastasierten Stadium so gut wirksam sind, zeigte in der Phase-III-Studie ASSURE bei Patienten mit lokal fortgeschrittenen Tumoren eine adjuvante Behandlung mit Sunitinib oder Sorafenib keinen Vorteil gegenüber Placebo.
In die Phase-III-Studie S-TRAC wurden nur Patienten mit klarzelligem Nierenzellkarzinom eingeschlossen, die nephrektomiert worden waren und nach UISS ein hohes Rezidivrisiko, d. h. ein
T-Stadium von 3 oder 4 und/oder ein
N-Stadium von 1–2 aufwiesen. Wie Alain Ravaud, Bordeaux, in Kopenhagen berichtete [3, 4], erhielten sie randomisiert über maximal ein Jahr entweder Sunitinib oder Placebo. Die Anfangsdosierung des Kinaseinhibitors von 50 mg/d über jeweils vier Wochen mit zwei Wochen Pause konnte bei Auftreten von Nebenwirkungen auf 37,5 mg/d verringert werden.
Primärer Endpunkt war das zentral überprüfte krankheitsfreie Überleben, und hier ergab sich in der verblindeten zentralen Analyse der radiologischen Bilder ein signifikanter Vorteil für die Sunitinib-Gruppe (median 6,8 vs. 5,6 Monate; HR 0,761; p = 0,030). In zwei Landmark-Analysen waren nach drei Jahren 64,9% versus 59,5% und nach fünf Jahren 59,3% versus 51,3% der Patienten krankheitsfrei am Leben, d. h. der Abstand der Kurven scheint sich bisher nicht zu verkleinern (Abb. 3). Zum Gesamtüberleben ist noch keine Aussage möglich, in keinem der beiden Arme wurde bisher der Medianwert erreicht.
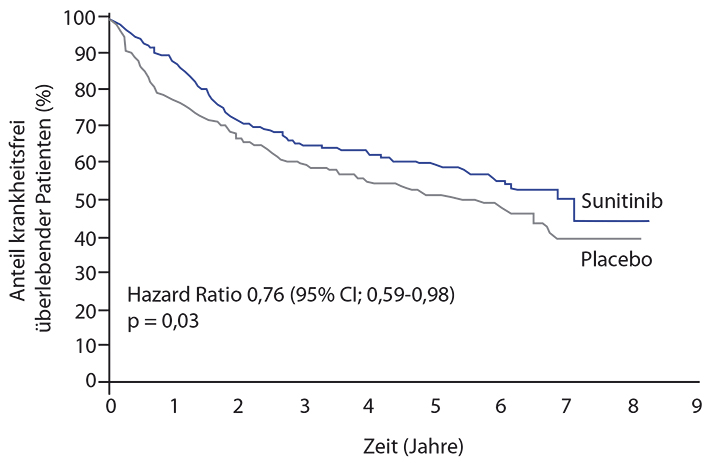
Grad-3/4-Nebenwirkungen traten im Sunitinib-Arm häufiger auf, gut ein Viertel der Patienten im Verum- und etwa 6% derer im Placeboarm beendeten die Behandlung aufgrund von Nebenwirkungen, unter Sunitinib v. a. wegen Hand-Fuß-Syndrom, Hypertonus, Asthenie, Fatigue, Lungenembolien und gastroösophagealem Reflux. Bei der Lebensqualität zeigte sich ein signifikanter Unterschied zuungunsten von Sunitinib lediglich bei Appetitverlust und Diarrhö.
Der hier gezeigte Vorteil ist nicht besonders groß, immerhin handelt es sich aber um die erste positive Studie zur adjuvanten Therapie des Nierenzellkarzinoms. Man kann auf weitere Untersuchungen in dieser Richtung gespannt sein.
Angriff auf Erstlinien-Standard Sunitinib
Nach Jahrzehnten der Stagnation gibt es heute zur Therapie des metastasierten Nierenzellkarzinoms mehr Therapieoptionen als für viele häufigere Tumoren. Jetzt ist offenbar die Zeit der Head-to-Head-Vergleiche gekommen: Bereits in der Erstlinie scheint bei Patienten mit weniger guter Prognose der neue Kinaseinhibitor Cabozantinib dem alten Standard Sunitinib überlegen zu sein, wie sich in der Phase-II-Studie CABOSUN zeigte.
Für diese Patienten mit intermediärem oder hohem Risiko fallen nämlich die Ergebnisse mit Sunitinib nicht so gut aus, ebenso bei Vorliegen von Knochenmetastasen. Die vermehrte Expression der Rezeptor-Tyrosinkinasen MET und AXL ist offenbar mit einer schlechteren Prognose und mit Resistenzen gegenüber herkömmlichen Tyrosinkinaseinhibitoren assoziiert. Da mit Cabozantinib für Patienten im Rezidiv seit Kurzem eine Substanz verfügbar ist, die neben den VEGF-Rezeptoren auch MET und AXL hemmt, sponserte das National Cancer Institute (NCI) der USA die randomisierte Phase-II-Studie CABOSUN, so Toni Choueiri, Boston [5]: Darin wurde Cabozantinib (60 mg/d in sechswöchigen Zyklen) bei 150 Patienten mit nicht vorbehandeltem Nierenzellkarzinom und intermediärem oder hohem Risiko direkt gegen Sunitinib (50 mg/d für vier Wochen, gefolgt von zwei Wochen Pause) getestet.
Ein Cross-over war nicht gestattet, primärer Endpunkt war das progressionsfreie Überleben, und hier erwies sich Cabozantinib mit median 8,2 gegenüber 5,6 Monaten als signifikant überlegen (HR 0,69; p = 0,012). Dies war unabhängig von der Risikogruppe (intermediär oder Hochrisiko) und ganz besonders deutlich für Patienten mit Knochenmetastasen, die unter anderen Inhibitoren eine schlechte Prognose haben.
Auch beim sekundären Endpunkt Ansprechen war Cabozantinib deutlich überlegen (46% vs. 18%); mit 87,3% der Patienten erzielten doppelt so viele darunter eine Größenreduktion ihrer Tumorläsionen wie unter Sunitinib (43,6%), so Choueiri. Beim sekundären Endpunkt Gesamtüberleben war Cabozantinib mit median 30,3 versus 21,8 Monaten zumindest numerisch überlegen, auch wenn der Unterschied noch nicht signifikant ausfiel.
Bei der Toxizität waren beide Substanzen vergleichbar: Nebenwirkungen vom Grad 3 gab es bei 58% der Patienten im Cabozantinib- und bei 60% derer im Sunitinib-Arm; auch bei Grad-4- und Grad-5-Nebenwirkungen war das Verhältnis mit 8% versus 8% bzw. 5% versus 4% ausgeglichen.
Cabozantinib stellt damit, so Choueiri, eine potenzielle neue Behandlungsoption für Patienten mit fortgeschrittenem, noch nicht behandeltem Nierenzellkarzinom dar.
Neuer Ansatz zur Apoptose-Induktion beim Prostatakarzinom enttäuschend
In die Therapie des metastasierten, kastrationsresistenten Prostatakarzinoms sind in den letzten Jahren mehrere Substanzen neu eingeführt worden (Cabazitaxel, Abirateron, Enzalutamid, Radium-223). Von der Hemmung des zytoprotektiven und anti-apoptotischen Proteins Clusterin hat man sich ebenfalls viel versprochen, aber der Clusterin-Inhibitor Custirsen konnte in der Zweitlinientherapie in der AFFINITY-Studie nicht überzeugen, wie Karim Fizazi, Villejuif, in Kopenhagen erläuterte [6].
Viele Anti-Tumor-Therapien führen zu einer Hochregulierung der Expression von Clusterin. Das Antisense-Oligonukleotid Custirsen kann in Zellkulturen und in Tiermodellen die Expression von Clusterin blockieren und in Tumorzellen die Apoptose induzieren. Außerdem erhöht es die Sensitivität von Prostatakarzinomzellen gegenüber Taxanen und verlängerte in einer randomisierten Phase-II-Studie in Kombination mit Docetaxel das Gesamtüberleben gegenüber der alleinigen Taxan-Therapie. In der Phase-III-Studie SYNERGY zur Erstlinientherapie war dieses Konzept ebenfalls wirksam, allerdings bei Patienten mit schlechter Prognose. In der Therapie vorbehandelter Patienten, die in der Phase-III-Studie AFFINITY von Fizazi und Kollegen untersucht wurden, war das Ergebnis aber enttäuschend:
Insgesamt 635 mit Docetaxel vorbehandelte und progrediente Patienten erhielten maximal zehn Zyklen Cabazitaxel und Prednison und wurden randomisiert, zusätzlich entweder Custirsen oder keine weitere Therapie zu bekommen. Bei etwas über 60% der Patienten in beiden Armen war die Prognose schlecht, aber auch sie profitierten bezüglich des Gesamtüberlebens nicht von Custirsen (median 11,1 vs. 10,9 Monate; HR 0,918; p = 0,235).
Der Clusterin-Inhibitor ist gut verträglich, es traten kaum mehr Nebenwirkungen vom Grad 3–4 auf als im Kontrollarm. Die mangelnde Wirksamkeit war auch nicht durch die Folgetherapien zu erklären: Ungefähr gleich viele Patienten in beiden Armen hatten im Anschluss noch andere wirksame Therapien wie Cabazitaxel, Enzalutamid oder Abirateron erhalten.
Eine mögliche Erklärung für den Misserfolg ist laut Fizazi, dass die verwendeten Dosierungen das Zielmolekül Clusterin nicht ausreichend hemmen: So überlebten in einer Landmark-Analyse im experimentellen Arm die Patienten länger, bei denen die Clusterin-Titer im Serum unter der Behandlung stärker abfielen. Die Entwicklung der Substanz geht jedenfalls weiter: In der ENSPIRIT-Studie erhalten vorbehandelte Patienten mit nicht-kleinzelligem Lungenkarzinom randomisiert Docetaxel mit oder ohne Custirsen. Die ersten Ergebnisse werden gegen Ende des Jahres erwartet.
Josef Gulden
Literatur
1. Galsky MD et al. ESMO 2016, Abstract #LBA31_PR.
2. Balan A et al. ESMO 2016, Abstract #LBA32_PR.
3. Ravaud A et al. ESMO 2016, Abstract #LBA11_PR.
4. Ravaud A et al. N Engl J Med 2016, Oct 10 [prepub ahead of print, DOI 10.1056/NEJMoa1611406].
5. Choueiri T et al. ESMO 2016, Abstract #LBA30_PR.
6. Fizazi K et al. ESMO 2016, Abstract #LBA09_PR.

