Pathophysiologie
Als Akutphasen-Protein ist VWF bei verschiedenen Erkrankungen erhöht, zum Beispiel bei der akuten koronaren Herzerkrankung, Schlaganfall, Atherosklerose, Kollagenosen, rheumatischen Erkrankungen, Vaskulitiden, Malignomen und nach Transplantationen. Mit VWF steigen auch die Spiegel von FVIII und begünstigen die Thrombinbildung. Eine aktuelle Studie zeigt einen Zusammenhang von Thrombosen bei Tumorpatienten mit erhöhten Werten von VWF[6].
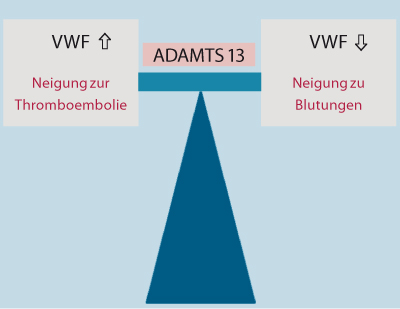
Erhöhte Spiegel von VWF – insbesondere von UL-VWF – begünstigen Venenthrombosen, Myokardinfarkt und Schlaganfälle. UL-VWF steigt an, wenn die Aktivität von ADAMTS 13 reduziert ist, u. a. bei den obengenannten Erkrankungen sowie bei Sepsis oder Tumoren. Oxidative Veränderungen bei Entzündungen oder im Bereich atherosklerotischer Plaques sowie freies Hämoglobin verhindern die Spaltung von VWF durch ADAMTS 13. Niedrige Spiegel von ADAMTS13 sind daher ein Risikofaktor für koronare Herzerkrankungen[7].
Die Bedeutung von ADAMTS 13 zeigt sich auch eindrucksvoll bei Mikroangiopathien wie der thrombotischen thrombozytopenischen Purpura (TTP) mit Thrombosen in der Mikrozirkulation bis hin zum Organversagen. Ursache dafür ist die ausgebliebene oder reduzierte Spaltung der VWF-Multimere durch eine niedrige Aktivität von ADAMTS 13 (durch Mutation, Synthesestörung oder Autoantikörper verursacht), sodass es zu einer Anhäufung von besonders großen, thrombogenen Multimeren kommt[8]. Beim akuten Herzinfarkt fand man direkt hinter dem stenosierten Bereich der Koronargefäße eine lokal geringere ADAMTS 13-Aktivität und damit ein Ungleichgewicht zwischen ADAMTS 13 und VWF[9].
Einige genetische Varianten von ADAMTS 13 sind mit dem Risiko für Schlaganfall bei Kindern assoziiert[10]. ADAMTS 13 spielt auch eine Rolle in der Regulation der Entzündung und der Angiogenese sowie im Abbau von extrazellulärer Matrix.
Therapie des VWS
Die Behandlung von VWF-Patienten erfolgt meist in speziellen Zentren oder Praxen. Oft reicht bei VWS Typ 1 eine Gabe des Hormons Desmopressin (DDAVP), das die Freisetzung von körpereigenem VWF aus dem Endothel induziert.
In schweren Fällen werden VWF-Konzentrate verwendet. Die Präparate unterscheiden sich in Bezug auf Reinheit und insbesondere FVIII-Gehalt und müssen anhand der jeweiligen Diagnose und Risiken individuell ausgesucht werden.
Antifibrinolytika werden oft zusätzlich eingesetzt. Globaltests eignen sich zum Monitoring[12]. Eine rekombinante Form von ADAMTS 13 ist in der klinischen Entwicklung. Im Tiermodell zeigten sich gute Ergebnisse bei TTP und beim ischämischen Schlaganfall, insbesondere bei Verschlüssen, die gegen das derzeitig einzige für diese Indikation zugelassene Thrombolytikum t-PA resistent waren[12]. Solche Verschlüsse enthalten sehr viel VWF. Gegen erhöhte Spiegel von VWF gibt es derzeit keine spezifische Therapie, allerdings haben Statine eine gewisse Wirkung[13].
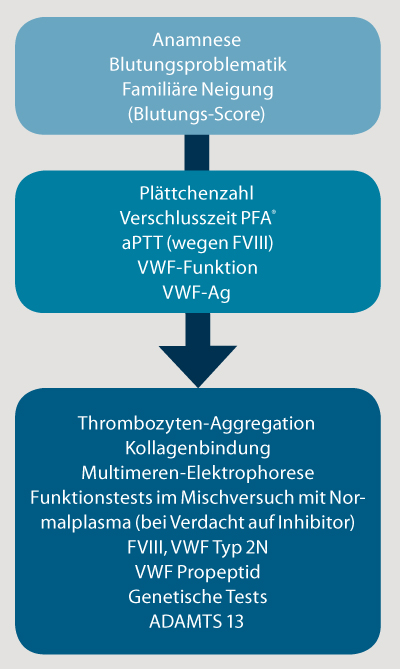
Basisanalytik
Eine sorgfältige Anamnese mit Erhebung eines Blutungs-Scores[14] und eine Labordiagnostik unter Einsatz verschiedener Methoden (Abb. 2) sind wichtig für eine fundierte Diagnose und Therapie. Sowohl erniedrigte wie auch erhöhte Werte von VWF haben Relevanz, wobei bisher meist die Abklärung eines Mangels im Vordergrund steht. Ein Blutbild ist unabdingbar, da manche Formen des VWS auch zu pathologischen Thrombozytenzahlen oder -größen führen. Einen ersten Hinweis auf einen VWF-Mangel kann eine verlängerte Verschlusszeit im PFA liefern[15]. Dieser einfache Vollblutglobaltest hängt relativ stark von VWF ab, aber auch von anderen Faktoren. Achtung: Übliche Gerinnungstests erfassen VWF gar nicht (TPZ) oder nur indirekt (aPTT) über die oft erniedrigten FVIII-Spiegel bei VWS-Patienten. Bei einer pathologischen aPTT sollte daher immer an die Möglichkeit eines VWF-Mangels gedacht werden.
Automatisierbare Tests für Konzentration (VWF-Ag) und Funktion des VWF sind auf Gerinnungsgeräten mit guter Reproduzierbarkeit und Sensitivität verfügbar und eignen sich prinzipiell für alle Labors. Quotienten aus VWF-Ag und Funktion können einen Verdacht auf einen qualitativen VWF-Mangel liefern (Tab. 2). Bei der Interpretation ist stets zu berücksichtigen, dass Träger der Blutgruppe 0 niedrigere Werte von VWF zeigen als A, B oder AB Zudem steigt VWF mit dem Alter[16].
Bei Werten im Grenzbereich ist eine neue Blutentnahme an einem anderen Tag sinnvoll, da der Spiegel von VWF schwanken kann. Nur wirklich niedrige Spiegel von VWF (< 20–30%) sind klinisch relevant im Sinne einer Blutungsneigung; eine Überdiagnose ist zu vermeiden, insbesondere beim Typ 1[17]. Bei vielen Patienten mit leicht verminderten VWF-Werten ist oft nicht sicher, ob sie wirklich ein VWS haben.
Weiterführende Tests
Die wichtigste Methode, die eine definitive Charakterisierung eines VWF-Syndroms erlaubt, ist die Multimeren-Elektrophorese, die die verschiedenen Größen der VWF-Multimere darstellt[18]. Diese ist sehr komplex und zeitaufwendig und bleibt daher bisher auf wenige Zentren beschränkt. Eine neue, erheblich schnellere Methode für übliche Elektrophoresegeräte ist demnächst verfügbar.
Wegen der wichtigen Rolle in der Interaktion mit Thrombozyten und der thrombozytären Form von VWF wird bei Verdacht auf ein VWS meist die Thrombozytenaggregation untersucht. Bei Mangel an VWF findet man mit Kollagen oft einen pathologischen Wert, ebenso mit Ristocetin, das VWF an den GP-1b-Komplex der Plättchen bindet und eine Agglutination auslöst. Bei VWS Typ 2B beobachtet man mit Ristocetin eine gesteigerte Aktivität. Die Untersuchung der Kollagenbindungsfähigkeit von VWF rundet diese Untersuchungen ab. Immer öfter werden Patienten mit VWS auch genetisch charakterisiert.
Ein besonderer Typ des VWF-Mangels ist Typ 2N, der Defekt der Bindungsstelle für FVIII, wo der FVIII-Spiegel bis auf unter 10% sinken kann. Für VWF 2N ist ein ELISA-Test erhältlich.
Für die Bestimmung von ADAMTS13 stehen bisher noch keine automatisierten und insbesondere keine notfalltauglichen Tests zur Verfügung, obwohl die Bedeutung dieses Parameters weit über das VWS hinausgeht. Die Analytik der Konzentration und von Antikörpern gegen ADAMTS13 erfolgt mit ELISA. Funktionelle Tests verwenden überwiegend fluorogene Tests in ELISA-ähnlichen Formaten.
Ausblick
VWF ist in der Mikrozirkulation ganz entscheidend für Reparaturvorgänge, aber auch für unerwünschte Verschlüsse von der Thrombose bis hin zum Organversagen. Konzentrationsänderungen – gerade auch erhöhte Werte und umso mehr geänderte Molekülgrößen – haben eine hohe Relevanz und prognostischen Wert, werden aber oft nicht ausreichend untersucht und berücksichtigt. Hier kann das Labor einen wichtigen Beitrag leisten.

