Die personalisierte Lungenkrebstherapie feiert dieses Jahr ein bedeutsames Jubiläum: Vor zehn Jahren wurde mit Gefitinib erstmals ein Tyrosinkinase-Inhibitor (TKI) zur zielgerichteten Erstlinientherapie des fortgeschrittenen, nicht-kleinzelligen Lungenkarzinoms (NSCLC) mit aktivierender EGFR-Mutation zugelassen. Da das Vorliegen der Mutation Voraussetzung für das Therapieansprechen war [1, 2], wurde die molekularpathologische Diagnostik vor dem Einsatz in der Behandlung eines metastasierten NSCLC im Rahmen der Zulassung zwingend gefordert [3]. Es handelte sich damit um das erste personalisierte Therapiekonzept beim Lungenkarzinom.
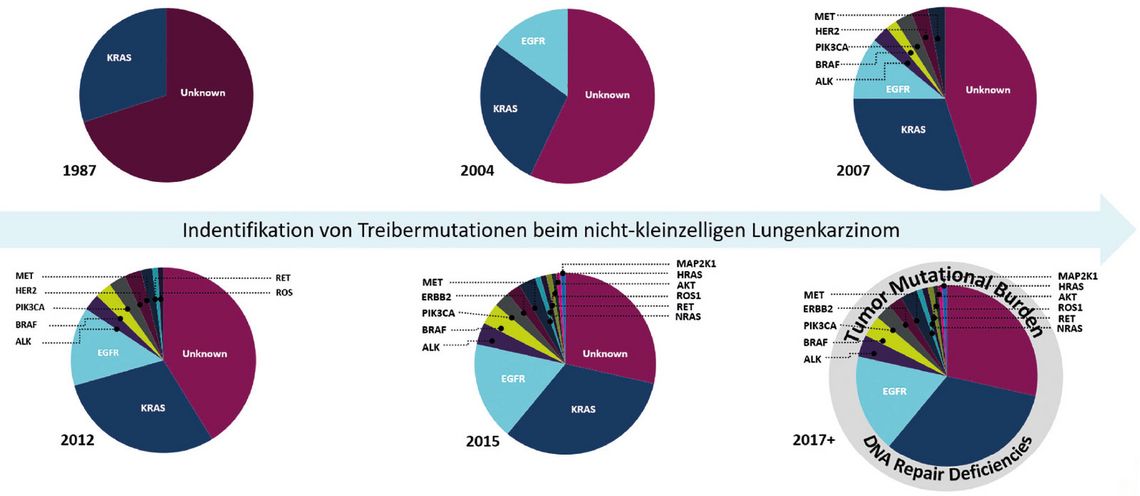
Inzwischen hat die Anzahl bekannter genomischer Veränderungen sowie personalisierter Therapieschemata stark zugenommen [z. B. 3]: Waren bis zur Jahrtausendwende beim NSCLC nur die nicht therapeutisch adressierbaren KRAS-Mutationen als ursächliche Treiber bekannt, so kann man heute routinemäßig eine ganze Reihe von Genen auf therapierelevante Punktmutationen, Deletionen, Insertionen, Fusionen und Translokationen untersuchen; zusätzlich kann die genomische Instabilität (Mikrosatelliteninstabilität, MSI) und die Gesamtmutationslast (Tumor Mutatinal Burden, TMB) bestimmt werden. Abb. 1 zeigt, dass dadurch der Anteil molekular klassifizierbarer Lungenkarzinome in den letzten Jahren auf mehr als zwei Drittel zunahm, wobei weiterhin nicht alle gezielt therapierbar sind; ein prominentes Beispiel hierfür sind die KRAS-mutierten Adenokarzinome, für die noch keine Target-spezifischen Wirkstoffe zur Verfügung stehen. Studien zeigen immer wieder auch hier vielversprechende Ansätze, ohne dass es bislang zu einer Zulassung kam. Hinzu kommt die Notwendigkeit einer immunhistochemischen Bestimmung der PD-L1-Expression als Entscheidungsgrundlage für eine mögliche Immuntherapie, falls keine therapeutisch adressierbare genetische Veränderung nachweisbar ist.