CLL: BTK-Inhibitor auch in Erstlinie deutlich überlegen
Die chronische lymphatische Leukämie ist in den letzten Jahren zu einer Modellerkrankung für die Entwicklung zielgerichteter Therapien geworden. Zwei neue Klassen von Medikamenten, Inhibitoren von Bruton-Tyrosinkinase (BTK) und der Phosphaditylinositol-3-Kinase (PI3K), sind bei B-Zell-Lymphomen generell wirksam, wurden aber zum ersten Mal überhaupt zur Behandlung der rezidivierten oder refraktären CLL zugelassen.
Der BTK-Inhibitor Ibrutinib (Imbruvica®) war in dieser Indikation in der RESONATE-Studie [1] erheblich wirksamer als der CD20-Antikörper Ofatumumab in Monotherapie – sowohl bei den Ansprechraten als auch beim progressionsfreien und Gesamtüberleben, so Prof. Jan Dürig, Essen. Diese Überlegenheit war in allen untersuchten Subgruppen, unabhängig von Alter, Geschlecht, Vorbehandlungen, Krankheitslast, Zytogenetik etc., erkennbar. Auch in Kombination mit einer herkömmlichen Chemoimmuntherapie, nämlich mit Bendamustin-Rituximab (BR) war Ibrutinib in der HELIOS-Studie [2] der alleinigen BR-Behandlung überlegen: Lediglich beim Gesamtüberleben war der Unterschied mit einer Hazard Ratio von 0,628 zwar beachtlich, nach median 17 Monaten Nachbeobachtungszeit aber noch nicht ganz signifikant (p = 0,0598).
Mit der beim letzten ASH-Kongress im Dezember 2015 erstmals vorgestellten RESONATE-2-Studie [3, 4] dürfte Ibrutinib auch in die Erstlinientherapie Einzug halten, so Prof. Stephan Stilgenbauer, Ulm: Eine Monotherapie mit dem Inhibitor wurde hier bei Patienten mit neu diagnostizierter CLL, die nicht für eine Fludarabin-haltige Behandlung infrage kamen, randomisiert gegen Chlorambucil getestet. Primärer Endpunkt war das progressionsfreie Überleben, und hier war der Medianwert im Ibrutinib-Arm noch nicht erreicht, während er im Chlorambucil-Arm 18,9 Monate betrug; zum 18-Monats-Zeitpunkt waren 90% der Patienten unter Ibrutinib versus 52% derer im Kontrollarm progressionsfrei am Leben (Hazard Ratio 0,16; p < 0,0001; Abb. 1). Auch Hochrisiko-Patienten mit Deletion 11q bzw. mit unmutiertem IGHV-Status profitierten von der Therapie mit dem BTK-Inhibitor: Insbesondere scheint der Mutationsstatus keine negative prognostische Bedeutung mehr zu haben.
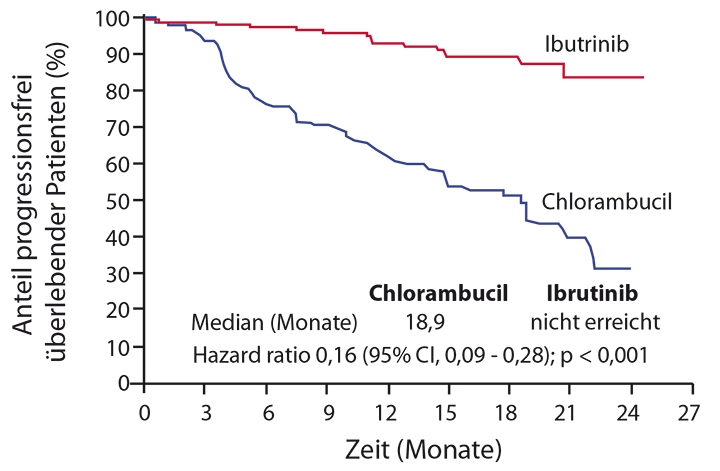
Auch beim Gesamtüberleben war Ibrutinib bereits in der Erstlinie hochsignifikant überlegen mit einer Überlebensrate von 98% nach zwei Jahren gegenüber nur 84% unter Chlorambucil (HR 0,16; p = 0,001). 90% der Patienten sprachen auf Ibrutinib an (10% mit einer Komplettremission), auf Chlorambucil nur 35% (5% komplett); nach acht Monaten lagen die Ansprechraten noch bei 82% versus 30%.
Die Verträglichkeit von Ibrutinib war gut: Die häufigsten Nebenwirkungen, bei mehr als 20% der Patienten beobachtet, waren Diarrhö, Fatigue, Husten und Nausea. Innerhalb der bisher ungefähr anderthalbjährigen Nachbeobachtungszeit wurden im Ibrutinib-Arm bei sechs Patienten Blutungen registriert (einmal Grad 2, viermal Grad 3 und einmal Grad 4); drei dieser sechs Patienten hatten zuvor eine Behandlung mit niedermolekularem Heparin, Azetylsalizylsäure oder Vitamin E erhalten, drei mussten wegen der Blutungen die Therapie beenden. Insgesamt nahmen 87% der Patienten Ibrutinib noch am Ende des Studienzeitraums ein.
Josef Gulden
Literatur
1. Byrd J et al. N Engl J Med 2014; 371: 213-23.
2. Chanan-Khan A et al. ASCO 2015, Abstract #LBA7005.
3. Tedeschi A et al. ASH 2015, Abstract #495.
4. Burger J et al. N Engl J Med 2015; 373: 2425-37.
Satellitensymposium „Therapie der chronischen lymphatischen Leukämie heute und morgen“ beim 32. Deutschen Krebskongress am 24.2.2016 in Berlin, unterstützt von Janssen-Cilag GmbH, Neuss.

