2nd Immunotherapy of Cancer Conference (ITOC-2)
Beim fortgeschrittenen Nierenzellkarzinom zeigen die neuen, bislang noch nicht zugelassenen Checkpoint-Inhibitoren erstaunliche Wirksamkeit. Da Angiogenese-Inhibitoren wie Hemmstoffe des vaskulären endothelialen Wachstumsfaktors (VEGF) und seiner Rezeptortyrosinkinasen (VEGFR-TKI) seit Jahren zu den wichtigsten Medikamenten bei diesem Tumor zählen, bietet es sich an, die Kombination beider Prinzipien zu untersuchen, so Hans Joerg Hammers, Baltimore.
VEGF spielt beim Nierenzellkarzinom eine wichtige Rolle und wirkt außerdem immunsuppressiv: Er hemmt die Reifung und die Funktion dendritischer Zellen und fördert andererseits die immunsuppressiven regulatorischen T-Zellen und „Myeloid-derived Supressor Cells“ (MDSC). Außerdem stimuliert er die Expression inhibitorischer Checkpoint-Moleküle auf CD8-positiven T-Zellen und bremst deren Eindringen ins Tumorgewebe. In präklinischen Modellen war eine Kombination beider Ansätze stark synergistisch, und das wurde bisher in zwei klinischen Phase-I-Studien überprüft:
- Patienten mit fortgeschrittenem Nierenzellkarzinom, die bereits VEGFR-TKI, aber keine Checkpoint-Inhibitoren erhalten hatten, wurden mit dem PD-1-Antikörper Nivolumab in Kombination mit Sunitinib (wenn sie vorher bereits Pazopanib bekommen hatten) oder Pazopanib (wenn sie vorher bereits mit Sunitinib behandelt worden waren). Nach sechs Wochen hatten 40–55% der auswertbaren Patienten angesprochen, anhaltende Remissionen sind nach über einem Jahr Nachbeobachtungszeit in der Sunitinib-Gruppe bei 59%, in der Pazopanib-Gruppe bei 33% zu erkennen; vier von 17 Patienten im Sunitinib-Arm sind auch nach Absetzen der Therapie noch in Remission. Renale und hepatische Toxizitäten waren unter diesen Kombinationen häufiger als unter den Einzelsubstanzen, aber handhabbar.
- In einer Phase-Ia-Studie erhielten Patienten mit fortgeschrittenen Tumoren verschiedener Histologien, darunter zehn mit Nierenzellkarzinomen, den PD-L1-Antikörper MPDL3280A und den VEGF-Antikörper Bevacizumab. Vier der zehn Patienten sprachen objektiv an, weitere fünf zeigten eine Krankheitsstabilisierung. CD8-positive T-Zellen wanderten nach der Gabe der Kombination ins Tumorgewebe ein. Es wurden keine Grad-4-Nebenwirkungen registriert, die man auf den PD-L1-Antikörper hätte zurückführen können.
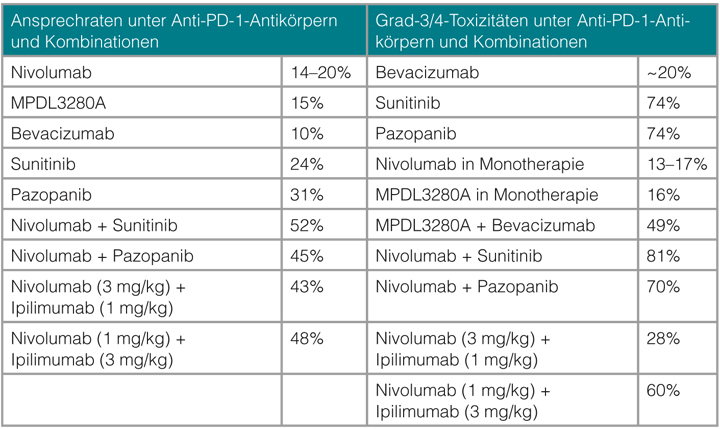
Die Nachbeobachtungszeiten sind noch kurz, deshalb lässt sich die Frage, ob Langzeitremissionen durch die Zuschaltung der Anti-Angiogenese häufiger werden, derzeit noch nicht schlüssig beantworten. Die Ansprechraten sind mit den Kombinationen jedenfalls deutlich höher, ebenso aber auch die Toxizitäten (s. Tab. 1). In Phase-I- und Phase-II-Studien werden zahlreiche weitere Kombinationen aus Checkpoint-Inhibitoren und anti-angiogenen Substanzen getestet. Dabei muss man jedoch vorsichtig vorgehen, so Hammers, weil vor allem renale und hepatische Toxizitäten häufiger sind als mit weniger selektiven Hemmstoffen des VEGF-Signalwegs.

