Das multiple Myelom ist nach wie vor unheilbar, d.h. nahezu alle Patienten rezidivieren irgendwann oder werden sogar refraktär gegenüber allen konventionellen Therapien. Mit dem Histondeacetylase-Inhibitor (HDACi) Panobinostat steht ein neues Therapieprinzip für diese Patienten in den Startlöchern, das in Kombination mit Bortezomib und Dexamethason in einer großen Phase-III-Studie für eine signifikante Verbesserung von Ansprechen und progressionsfreien Überleben im Vergleich zu Bortezomib/Dexamethason/Placebo sorgte.
Für Patienten mit rezidiviertem oder therapierefraktärem multiplem Myelom müssen dringend neue, noch wirksamere Therapien entwickelt werden: Patienten, die gegenüber Bortezomib und immunmodulatorischen Substanzen (IMiDs) refraktär sind, überleben im Median nur mehr ungefähr neun Monate. Panobinostat ist ein HDACi, der in geringen Konzentrationen mehrere Histondeacetylasen hemmt, darunter die vom Typ 6, die in Myelomzellen eine wichtige Rolle spielt. In Monotherapie zeigte Panobinostat (und auch andere HDACi) kaum Wirkung beim multiplen Myelom, aber unter der Kombination von Panobinostat mit dem Proteasominhibitor Bortezomib kommt es zu einer Akkumulation defekter Proteine in der Myelomzelle und letztlich zu ihrem Tod durch Apoptose.
In der Phase-III-Studie PANORAMA-1, deren erste Resultate Paul Richardson, Boston, bei der ASCO-Jahrestagung präsentierte, wurden deshalb 768 Patienten mit Bortezomib und Dexamethason behandelt und bekamen zusätzlich randomisiert entweder Placebo oder Panobinostat [1]. Zuerst wurden acht dreiwöchige Zyklen gegeben, wenn daraus wenigstens eine Krankheitsstabilisierung resultierte, kamen vier weitere sechswöchige Zyklen hinzu. Über 40% der Patienten waren mit Bortezomib, etwa ein Viertel mit Bortezomib und einem IMiD vorbehandelt.
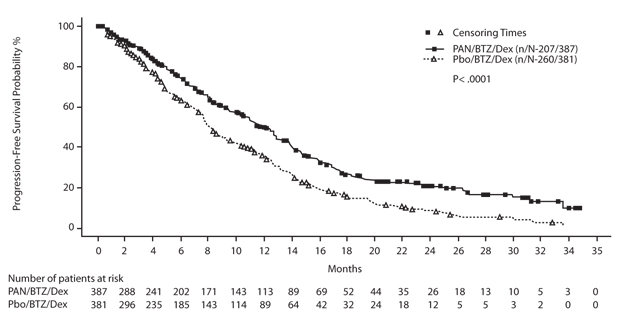
Die Patienten in der Panobinostat-Gruppe waren beim primären Endpunkt progressionsfreies Überleben mit median 12,0 gegenüber 8,1 Monaten deutlich im Vorteil, so Richardson (Hazard Ratio 0,63; p < 0,0001; Abb.). Diese Überlegenheit von Panobinostat fand sich in allen untersuchten Subgruppen, auch bei Patienten mit Hochrisiko-Zytogenetik (HR 0,47) sowie bei den zuvor therapierefraktären Patienten (HR 0,54).
Das Ansprechen insgesamt war nicht unterschiedlich, aber bei der Tiefe der erreichten Remissionen unterschieden sich beide Arme hochsignifikant: 27,6% der Patienten kamen mit Panobinostat in eine komplette oder beinahe komplette Remission, hingegen nur 15,7% mit Placebo (p = 0,00006). Panobinostat war mit Diarrhö und Fatigue vom Grad 3 oder 4 bei ungefähr jedem vierten Patienten assoziiert, 17,6% erlitten eine periphere Grad-3/4-Neuropathie. Nur 4,5% der Patienten aber brachen wegen einer Diarrhö, 2,9% wegen Fatigue die Therapie ab. Außerdem zeigte sich bei 67,4% der Patienten in der Verumgruppe eine Thrombozytopenie vom Grad 3 oder 4, aber lediglich 1,6% beendeten die Behandlung deswegen. Die Verträglichkeit der Kombination lässt sich Richardson zufolge mit ziemlicher Sicherheit noch verbessern: Bortezomib war hier intravenös gegeben worden, aber die subkutane Applikationsform, die mittlerweile zur Verfügung steht, sowie neue, weniger dosisdichte Applikationsschemata dürften die Neuropathie-Rate erheblich reduzieren.
Ein um vier Monate und fast 50% verlängertes medianes progressionsfreies Überleben bedeutet bei diesen stark vorbehandelten Myelom-Patienten einen erheblichen Fortschritt – zumal die hohe Aktivität auch in den Hochrisikogruppen zu sehen ist.
Josef Gulden
Literatur
1. Richardson PG et al. J Clin Oncol 2014; 32 (15S): 541s (ASCO 2014, Abstract #8510^).
Annual Meeting of the American Society of Clinical Oncology (ASCO), 30.5.-3.6.2014 in Chicago

