ASCO 2014 – Gastrointestinale Tumoren
Bei den gastrointestinalen Tumoren gab es beim diesjährigen ASCO-Kongress eine bunte Mischung aus unentschiedenen, negativen und positiven Studien. Unsere kleine Auswahl repräsentiert alle diese Typen und einen Großteil der im Verdauungstrakt vorkommenden Tumorentitäten.
Sicher am meisten erwartet worden war die erste Auswertung der US-amerikanischen CALGB80405-Studie zur Erstlinientherapie des kolorektalen Karzinoms vom KRAS-Wildtyp, die Alan Venook, San Francisco, in der Plenarsitzung präsentierte [1]. Zur Erinnerung: Die deutsche FIRE-3-Studie und auch die randomisierte Phase-II-Studie PEAK hatten im direkten Vergleich eine Überlegenheit der EGFR-Antikörper Cetuximab bzw. Panitumumab gegenüber dem VEGF-Antikörper Bevacizumab – jeweils in Kombination mit Chemotherapie – beim Gesamtüberleben von Patienten mit vorher unbehandelten metastasierten kolorektalen Karzinomen gezeigt. In der CALGB-Studie war die Chemotherapie freigestellt gewesen (73,4% der Patienten hatten FOLFOX erhalten, die übrigen FOLFIRI), randomisiert war zusätzlich Cetuximab oder Bevacizumab gegeben worden. Ein Amendment hatte im Jahr 2008 die Rekrutierung auf Patienten mit KRAS-Wildtyp-Tumoren beschränkt.
Bei insgesamt sehr langen Überlebenszeiten – median 29 Monate mit Bevacizumab, 29,9 Monate mit Cetuximab, die laut Venook „einen neuen Maßstab in der Behandlung von Patienten mit kolorektalem Karzinom setzen“, war bei diesen insgesamt 804 Patienten mit KRAS-Wildtyp-Tumoren kein signifikanter Unterschied zwischen beiden Armen zu sehen (Hazard Ratio 0,925; p = 0,34). Allgemein wird das jedoch noch nicht als das letzte Wort zu diesem Thema angesehen: Der Referent war selbst sichtbar nicht ganz glücklich über die Qualität der Daten. Besonders schmerzhaft wurde das Fehlen von Angaben zu RAS-Mutationen neben denen im KRAS-Exon 2 empfunden: Auch der Diskutant Josep Tabernero, Barcelona, betonte, dass viele der Daten noch reifen müssten, insbesondere seien die zusätzlichen Biomarker-Analysen, v. a. die Angaben zum Pan-RAS-Status der Patienten, von Bedeutung, die durchaus noch messbare Änderungen in der Gewichtung der Ergebnisse bringen könnten. Unerklärbar ist beispielsweise derzeit auch, warum die Patienten, die als Chemotherapie FOLFIRI erhalten hatten, mit Bevacizumab tendenziell länger überlebt hatten, während in der FIRE-3-Studie (wo alle Patienten mit FOLFIRI behandelt worden waren) das Gegenteil, nämlich ein signifikanter Vorteil für Cetuximab zu sehen gewesen war. Man wird bis zur Präsentation der fehlenden Daten warten müssen, bevor man diese Ergebnisse abschließend beurteilen kann.
EGFR-Inhibitor bei Ösophaguskarzinom
Ein inoperables Ösophaguskarzinom wird in der Regel mit einer Radiochemotherapie behandelt, wobei 5-Fluorouracil plus Cisplatin bzw. ein Taxan und ein Platinsalz ungefähr gleichwertig zu sein scheinen. Da 60–80% der Ösophaguskarzinome den EGF-Rezeptor exprimieren und eine Pilotstudie eine Wirksamkeit für die Zugabe von Cetuximab zur Chemotherapie anzudeuten schien, führte die Radiation Therapy Oncology Group (RTOG) eine Phase-III-Studie durch, in der 328 Patienten mit inoperablem Ösophaguskarzinom eine Chemotherapie aus wöchentlich gegebenem Cisplatin und Paclitaxel und 50,4 Gy Bestrahlung in 28 Fraktionen sowie randomisiert zur Hälfte Cetuximab erhielten [3]. Die Studie wurde nach einer Interimsanalyse gestoppt, so David Ilson, New York: Zwar war das Überleben von Patienten, die eine klinische Komplettremission erreicht hatten, verlängert, aber ein Vorteil durch den EGFR-Antikörper hatte sich weder bei den Komplettremissionsraten noch beim primären Endpunkt Gesamtüberleben ergeben. Wenn das Prinzip der EGFR-Inhibition eine Zukunft in der Therapie des Ösophaguskarzinoms (und auch des Magenkarzinoms) haben sollte, so Ilson, müssten Biomarker identifiziert werden, anhand derer man (ähnlich wie mit den RAS-Mutationen beim kolorektalen Karzinom) diejenigen Patienten selektieren könnte, die tatsächlich davon profitieren.
Sorafenib unwirksam als adjuvante Therapie beim HCC
Der Tyrosinkinaseinhibitor Sorafenib ist nach wie vor die einzige zugelassene systemische Therapie des metastasierten oder lokal fortgeschrittenen hepatozellulären Karzinoms. Mehrere kontrollierte Studien haben einen signifikanten Überlebensvorteil gezeigt, und deshalb wurde in der Phase-III-Studie STORM untersucht, ob Sorafenib auch nach erfolgreicher lokaler Therapie in adjuvanter Gabe von Vorteil ist und die hohe Rezidivrate senken kann [4].
Die 1.114 eingeschlossenen Patienten waren nach Resektion oder lokal-ablativer Therapie mit kurativer Intention tumorfrei und mussten eine gute Leberfunktion aufweisen (97% von ihnen mit Child-Pugh A), so Jordi Bruix, Barcelona. Sie erhielten randomisiert entweder Sorafenib 400 mg zweimal täglich oder Placebo. Primärer Endpunkt war das rezidivfreie Überleben, aber hier zeigte sich nach einer medianen Nachbeobachtungszeit von vier Jahren ebenso wenig ein Unterschied zwischen beiden Armen (median 33,4 vs. 33,8 Monate; Hazard Ratio 0,94; p = 0,26; Tab. 1) wie bei der medianen Zeit bis zum Rezidiv (38,6 vs. 35,8 Monate; HR = 0,89; p = 0,12). Beim Gesamtüberleben sind die Medianwerte noch nicht erreicht, aber auch hier ist kein Unterschied erkennbar (HR 0,995; p = 0,48).
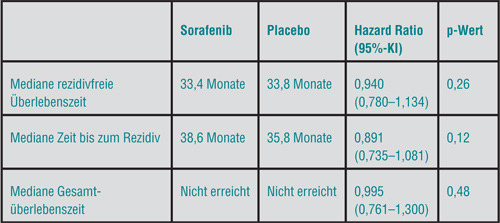
Die Nebenwirkungsrate war im Sorafenib-Arm doppelt so hoch wie im Placebo-Arm (94,1% vs. 46,4%), was zu einer höheren Abbruchrate (24% vs. 7%), einer beinahe halbierten Behandlungsdauer (12,5 vs. 22,2 Monate) und zu mehr Dosisreduktionen führte (mediane Tagesdosis 578 mg vs. 778 mg). Auch diese Studie ist daher als negativ zu bewerten, so Bruix; der Einsatzbereich von Sorafenib beschränkt sich damit weiterhin auf fortgeschrittene Stadien des Leberzellkarzinoms.
Ruxolitinib beim Pankreaskarzinom
Beim Pankreaskarzinom mit seiner nach wie vor desolaten Prognose ist jeder noch so geringe Therapiefortschritt willkommen. Die Tatsache, dass Pankreaskarzinome häufig mit systemischen Entzündungsreaktionen einhergehen, die auch eine noch schlechtere Prognose nach sich ziehen, ließ das Interesse an antiinflammatorisch wirksamen Therapieansätzen steigen. Ein bereits in der Klinik etabliertes Medikament, der zur Therapie der Myelofibrose zugelassene JAK-1/2-Inhibitor Ruxolitinib, reduziert Entzündungswerte und konnte in Kombination mit Capecitabin auch Aktivität in einem Tiermodell des menschlichen Adenokarzinoms des Pankreas zeigen. In dieser Konstellation, in Kombination mit Capecitabin, wurde Ruxolitinib deshalb in einer randomisierten und doppelblinden Phase-II-Studie gegen Capecitabin und Placebo getestet, so Herbert Hurwitz, Durham [5].
Beim primären Endpunkt Gesamtüberleben (Hazard Ratio 0,79; p = 0,25) ebenso wie beim progressionsfreien Überleben (HR 0,75; p = 0,28) war Ruxolitinib im Gesamtkollektiv der 127 teilnehmenden Patienten dem Placebo überlegen, wenn auch nicht signifikant (Tab. 2). Eine prospektiv geplante Subgruppenanalyse zeigte jedoch für die 60 Patienten mit einer bestehenden Entzündung, gemessen als ein Wert des C-reaktiven Proteins von > 13 mg/l, eine statistisch signifikante Halbierung des Mortalitätsrisikos (median 83 vs. 55 Tage; HR 0,47; p = 0,01). Auch wenn in einer multivariaten Analyse zahlreiche andere Variablen berücksichtigt wurden, blieb der Vorteil durch Ruxolitinib signifikant (HR 0,50; p = 0,037). Ebenfalls verlängert wurde das Überleben bei Patienten mit einem modifizierten Glasgow-Prognosescore von 1 bzw. 2, einem Maß für Entzündung bei Krebserkrankungen (HR 0,71 bzw. 0,49), wenngleich das wegen der niedrigeren Patientenzahlen nicht ganz signifikant ausfiel.
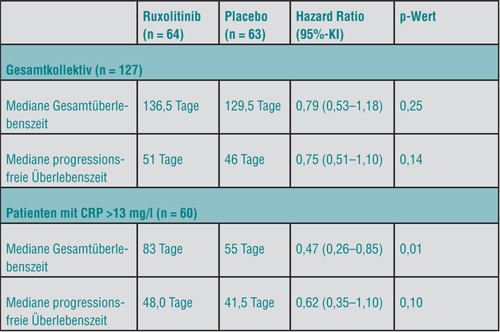
Die hier nachgewiesene Aktivität von Ruxolitinib, so Hurwitz, wird nun in zwei Phase-III-Studien (JANUS 1/2) bei Patienten mit Pankreaskarzinom und einem modifizierten Glasgow-Score von 1 und 2 überprüft. Drei Phase-II-Studien sollen darüber hinaus das Potenzial der Substanz bei kolorektalem Karzinom, nicht-kleinzelligem Lungenkarzinom und Mammakarzinom mit Entzündungszeichen eruieren.
Josef Gulden
Literatur
1. Venook AP et al. J Clin Oncol 2014; 32 (15S): 4s (ASCO 2014, Abstract #LBA3).
2. Ciardiello F et al. J Clin Oncol 2014; 32 (15S): 214s (ASCO 2014, Abstract #3506).
3. Ilson DH et al. J Clin Oncol 2014; 32 (15S): 256s (ASCO 2014, Abstract #4007).
4. Bruix J et al. J Clin Oncol 2014; 32 (15S): 256s (ASCO 2014, Abstract # 4006^).
5. Hurwitz H et al. J Clin Oncol 2014; 32 (15S): 255s (ASCO 2014, Abstract #4000).
Artikel als PDF downloaden

