Das Pankreaskarzinom gehört nach wie vor zu den desolatesten Diagnosen in der Onkologie mit einer medianen Überlebenszeit von unter einem Jahr. Nach fast sieben Jahren gab es im Dezember des vergangenen Jahres erstmals wieder eine Neuzulassung für diese Indikation: nab-Paclitaxel (Abraxane®) konnte in einer großen Phase-III-Studie die Überlebenszeit von Patienten mit metastasiertem Pankreaskarzinom signifikant um etwa zwei Monate verlängern.
Das Pankreaskarzinom weist ein besonders dichtes und schlecht vaskularisiertes Stroma auf, das zum einen Zytostatika von den Tumorzellen fernhält und zum anderen deren Wachstum fördert. Ungefähr vier von fünf dieser Tumoren exprimieren im Stroma das Albumin-bindende Protein SPARC (Secreted Protein Acidic and Rich in Cysteine), und die Expression zeigt eine negative Korrelation mit der Prognose der Patienten. Das ist die Rationale für den Einsatz von nab-Paclitaxel, so Prof. Michael Geißler, Esslingen: Aufgrund seiner Bindung an Albumin-Nanopartikel (nab) wird das Taxan über den endogenen transendothelialen Albumin-Transportweg, der Proteine wie gp60 und SPARC nutzt, selektiv in das Tumorgewebe aufgenommen und dort angereichert. Außerdem scheint nab-Paclitaxel das Stromagewebe aufzulockern und dadurch den Zugang auch für andere Zytostatika zu erleichtern.
Nach positiven Signalen in präklinischen und frühen klinischen Studien wurde dieser Ansatz in der multizentrischen randomisierten MPACT-Studie (Metastatic Pancreatic Adenocarcinoma Clinical Trial) in Kombination mit dem bisherigen Standard Gemcitabin gegen eine Gemcitabin-Monotherapie getestet, wie Prof. Volker Heinemann, München, berichtete: 861 Patienten mit metastasiertem Adenokarzinom des Pankreas, die zuvor keine Chemotherapie erhalten hatten, wurden randomisiert und bekamen entweder eine Gemcitabin-Monotherapie (1.000 mg/m2 zunächst an den Tagen 1, 8, 15, 22, 29, 36 und 43 eines ersten 56-Tage-Zyklus, dann in vierwöchigen Zyklen jeweils an den Tagen 1, 8 und 15) oder 125 mg/m2 nab-Paclitaxel, gefolgt von 1.000 mg/m2 Gemcitabin an den Tagen 1, 8 und 15 sowie 29, 36 und 43 eines ersten 56-Tage-Zyklus und an den Tagen 1, 8 und 15 der folgenden 28-Tage-Zyklen. Beide Therapien wurden jeweils bis zum Progress gegeben, primärer Endpunkt war das Gesamtüberleben.
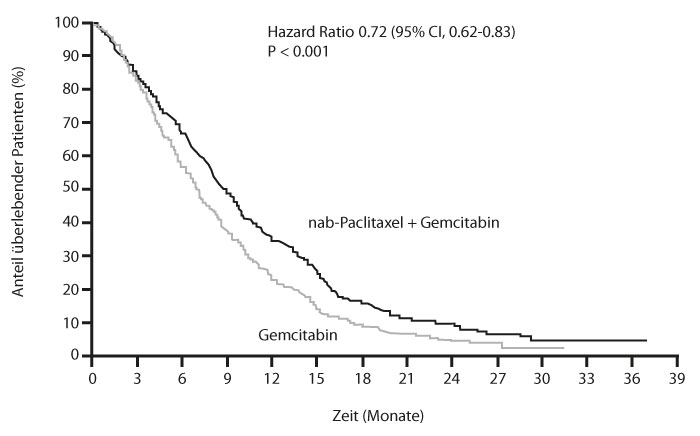
Dabei erwies sich die Kombination mit nab-Paclitaxel als deutlich überlegen: Die Patienten in der Verumgruppe überlebten median 8,7 Monate, die im Kontrollarm nur 6,6 Monate. Die Hazard Ratio lag bei 0,72, d. h. das Mortalitätsrisiko wurde durch nab-Paclitaxel um 28% reduziert (p < 0,0001). Nach einem Jahr waren in der Kontrollgruppe noch 22%, in der Kombinationsgruppe hingegen 35% der Patienten am Leben, was einem Zuwachs um 59% entspricht. Nach zwei Jahren lagen die Überlebensraten bei 10% versus 5%, nach drei Jahren lebten noch 4% der Patienten in der Kombinations-, aber kein einziger in der Kontrollgruppe mehr. Die Kombination war gut verträglich, so Heinemann: Die häufigsten Nebenwirkungen mit einem Schweregrad von 3 oder höher waren Neutropenien, Leukopenien, Fatigue und Neuropathien; letztere bildeten sich innerhalb von median einem Monat wieder zurück.
Die gute Verträglichkeit ist ein Faktor, der die neue Therapieoption besonders attraktiv macht: Eine ebenfalls sehr wirksame Behandlungsform, die Dreifachkombination aus 5-Fluorouracil, Irinotecan und Oxaliplatin (FOLFIRINOX), ist mit erheblichen Toxizitäten behaftet und kann deshalb nur Patienten in sehr gutem Allgemeinzustand gegeben werden, so Priv.-Doz. Dr. Helmut Oettle, Friedrichshafen. Für Patienten mit (tumorbedingten) Komorbiditäten und einem Karnofsky-Performancestatus von 70% oder mehr ist hingegen nab-Paclitaxel plus Gemcitabin die Therapie der Wahl. Subgruppenanalysen der MPACT-Studie zeigten nämlich, dass diese Kombination auch bei Patienten mit einem Karnofsky-Index zwischen 70 und 80% und bei solchen mit mehr als drei Metastasenlokalisationen das Überleben deutlich verlängern kann.
Auch für prognostisch ungünstige Patienten scheint nab-Paclitaxel plus Gemcitabin also eine hervorragende Option zu sein. Die hohe Remissionsrate von 23% (gegenüber nur 7% im Kontrollarm; p < 0,001) und die Tumorkontrollrate von 48% (vs. 33%; p < 0,001) lassen erwarten, dass nab-Paclitaxel bei der Weiterentwicklung der Therapiekonzepte gegen das Pankreaskarzinom eine wichtige Rolle spielen wird. In weiteren Studien wird untersucht, ob bei lokal fortgeschrittenen und primär inoperablen Tumoren ausreichende Remissionen erzielt werden können, um eine sekundäre Resektabilität und damit langfristig bessere Überlebenschancen zu ermöglichen. Außerdem wird das Nanopartikel-Taxan in der adjuvanten Therapie des primär operablen Pankreaskarzinoms geprüft.
Fortschritte finden in der Onkologie häufiger in kleinen Schritten als in großen Sprüngen statt. Die Einführung von nab-Paclitaxel wird im Allgemeinen zu keiner Heilung des Pankreaskarzinoms führen, stellt aber einen wesentlichen Fortschritt in der Therapie dieses prognostisch so überaus ungünstigen Tumors dar.
Martin Hoffmann
Fachpressegespräch „nab-Paclitaxel als neue Therapieoption beim metastasierten Pankreaskarzinom“ im Rahmen des Deutschen Krebskongresses am 20.2.2014 in Berlin, veranstaltet von
Celgene GmbH, München

